Comment développe-t-on un vaccin ?
Un vaccin sert à entraîner le système immunitaire à lutter contre un microbe qui peut provoquer une maladie grave ou mortelle. Le microbe peut être un virus, une bactérie ou même un parasite (dans le cas de la malaria, par exemple). Quelques heures après l’injection d’une dose de vaccin, les globules blancs spécialisés du système immunitaire – lymphocytes B et lymphocytes T – sont déjà activés. Et après environ 15 jours, les lymphocytes B libèrent dans le sang des anticorps capables de se fixer sur le microbe ciblé par le vaccin. Certains de ces anticorps neutralisent le microbe pour l’empêcher d’entrer dans les cellules humaines. D’autre part, des lymphocytes T (dits «tueurs») entrent en scène pour éliminer les microbes, afin qu’ils ne puissent pas provoquer de maladie ou de complications.
Pour que le système immunitaire puisse produire des lymphocytes B et T efficaces contre un microbe donné, il doit apprendre à reconnaître certains éléments caractéristiques de ce microbe: ce sont souvent des protéines spécifiques disposées sur la surface du microbe. Un vaccin contient toujours au moins ces éléments caractéristiques du microbe ciblé, qui peuvent être présentés au système immunitaire de plusieurs manières.
- Vaccins contenant le microbe en entier, sous forme atténuée. On parle de forme «atténuée» lorsqu’on manipule le microbe pour le rendre moins agressif, par exemple en réduisant sa capacité à se multiplier. C'est la méthode la plus efficace, mais aussi celle qui demande le plus de précautions. Les vaccins vivants atténués miment l’immunité naturelle et déclenchent une réponse immunitaire plus forte et prolongée: après 1 ou 2 doses, ils ne nécessitent pas de vaccination de rappel. Leur inconvénient principal est de ne pas pouvoir être administré (sauf exception) aux personnes dont le système immunitaire est affaibli par certaines maladies ou traitements médicaux.
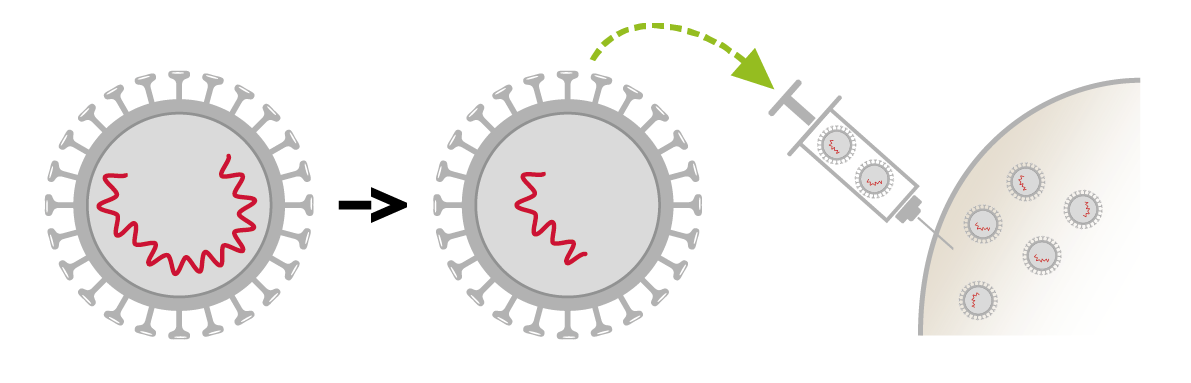
Les vaccins vivants atténués (ROR : Rougeole-Oreillons-Rubéole, varicelle, zona, fièvre jaune, rotavirus).
- Vaccins contenant le microbe en entier, sous forme inactivée. Le microbe est tué; il est totalement incapable de se multiplier et donc de provoquer une maladie. Les vaccins entiers inactivés sont généralement moins efficaces que les vaccins vivants atténués; ils nécessitent souvent plusieurs doses ou des rappels. Leur principal avantage est d’induire très peu d’effets secondaires et de pouvoir être administré même aux personnes dont le système immunitaire est affaibli.
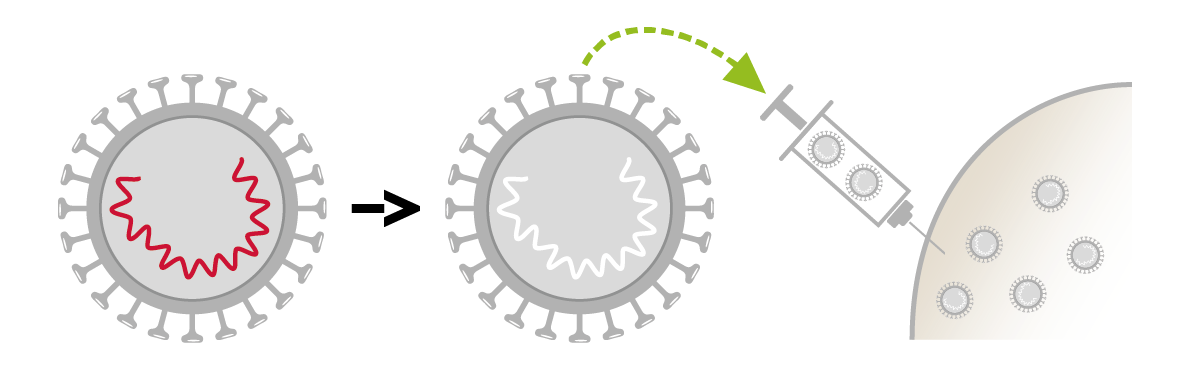
Les vaccins entiers inactivés (polio, hépatite A, méningo-encéphalite à tiques, méningocoques)
- Vaccins purifiés ne contenant qu’un ou plusieurs fragments du microbe. Ces vaccins contiennent uniquement les éléments du microbe nécessaires à sa reconnaissance par le système immunitaire pour une bonne protection. Ces vaccins ont l’avantage de stimuler le système immunitaire de manière très ciblée. Leur tolérance est donc excellente, mais des rappels sont souvent nécessaires. Vidéos de Swissmedic présentant le fonctionnement des vaccins à protéines.
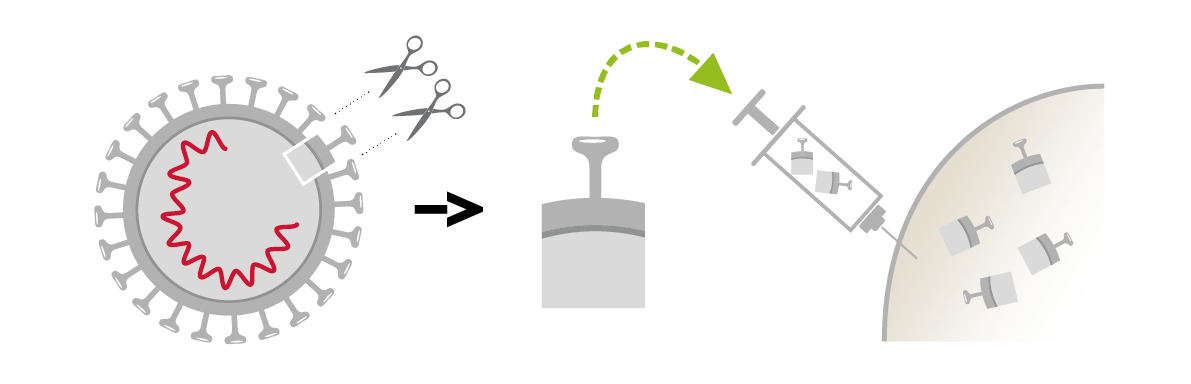
Les vaccins purifiés (diphtérie, tétanos, coqueluche, hépatite B, HPV, grippe, etc.)
- Vaccins conjugués contenant uniquement les sucres complexes (polysaccharides) de la capsule du microbe, fixés à une protéine de transport afin d'être mieux reconnus par le système immunitaire. Plusieurs injections sont parfois nécessaires pour obtenir l’immunité, qui ne dure parfois que quelques années.
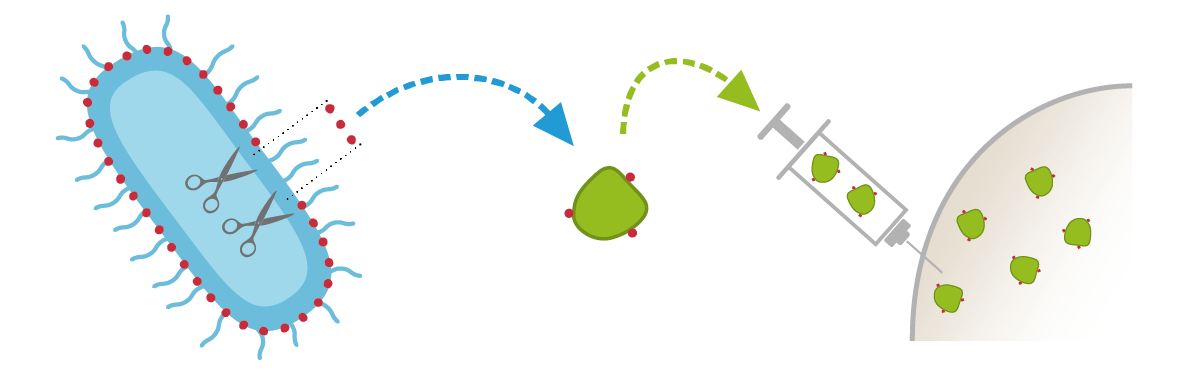
Les vaccins conjugués (Hib, pneumococoques)
- Vaccins à ARN messager, par injection directe d’un fragment du matériel génétique du microbe (ARN messager), encapsulé dans des nanoparticules composées de divers lipides (liposomes). La technologie des vaccins à ARN messager est connue depuis une dizaine d’années, mais malgré son attrait (simplicité de concept, rapidité de développement, facilité de production) elle n'a pas pu bénéficier des investissements nécessaires avant la mobilisation résultant de la pandémie de COVID-19.
Comparaison entre l'infection naturelle du coronavirus et la vaccination avec un ARN-messager (schémas simplifiés)
A. Infection naturelle
1. Un coronavirus SARS-CoV-2 pénètre dans l'organisme humain, puis se fixe sur une cellule grâce à ses protéines de surface en forme de clou (en anglais, cette protéine est nommée Spike).
2. Le virus est absorbé par la cellule; il libère dans la cellule son ARN (code génétique qui contient toute l'information nécessaire à fabriquer ce même virus).
3. La cellule humaine utilise ses propres outils pour lire l'ARN viral et fabriquer, malgré elle, toutes les parties du virus (différentes sortes de protéines + ARN viral).
4. De nouveaux virus peuvent s'auto-assembler, puis être libérés dans le corps humain pour poursuivre la contamination...
Pour stopper la reproduction du virus, il faut attendre plusieurs jours pour que le système immunitaire du corps réagisse, et produise finalement des anticorps.
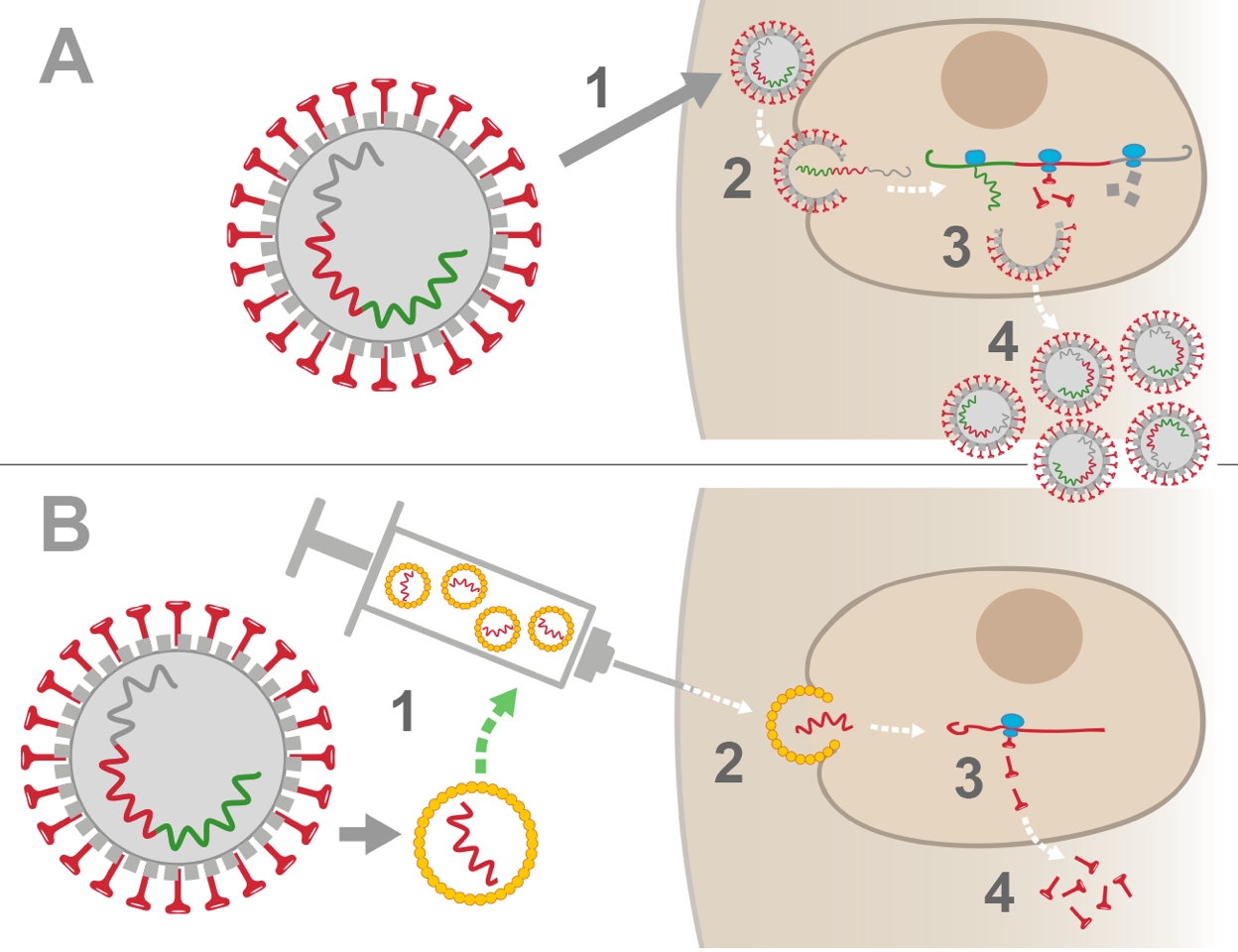
B. Vaccination par un ARN messager viral
1. En laboratoire, on fabrique des ARN-messagers codant seulement pour la protéine Spike du coronavirus. Les ARN-messagers sont insérés dans de petites bulles de graisse.
2. Lors de la vaccination, les bulles de graisses sont injectées dans le muscle du bras, puis elles sont absorbées par les cellules musculaires humaines: les ARN-messagers sont libérés.
3. La cellule humaine utilise ses propres outils pour lire l'ARN-messager et fabriquer uniquement des protéines Spike. Seules, ces protéines ne sont pas dangereuses pour l'organisme.
4. La cellule rejette des protéines virales Spike dans l'organisme – ce qui va alerter le système immunitaire et permettre au corps de produire des anticorps contre la protéine Spike…
2-3 semaines après la vaccination, si un coronavirus pénètre dans le corps, le système immunitaire saura le reconnaître rapidement et le neutraliser, notamment à l’aide d’anticorps contre la protéine Spike.
6. Vaccins «par vecteur» : un morceau important du microbe est inséré dans un virus ou dans une bactérie ne provoquant pas de maladie chez l’humain. Ces «vecteurs» sont choisis pour que leur multiplication soit impossible (p.ex. ChAdOx1) ou limitée (p.ex. rVSV) dans le corps humain afin de ne pas provoquer d’infection. Il s’agit d’une technique récente qui a déjà fait ses preuves pour la vaccination contre la maladie d’Ebola et contre certains cancers. Dans le cas des vaccins à vecteur viral reposant sur un adénovirus (vaccins d’Astra Zeneca/Université d’Oxford ou de Janssen/ Johnson&Johnson), le code génétique des adénovirus est modifié (ADN tronqué) pour que le virus ne puisse pas se répliquer dans le corps humain. Il est donc biologiquement exclu qu'il puisse provoquer une infection à adénovirus modifié. L’ADN de ces adénovirus utilisés comme vecteurs peut entrer dans les noyaux des cellules, mais son incorporation dans l'ADN des cellules humaines est rendue impossible par une modification des extrémités de ses brins d’ADN. L'ADN de ces adénovirus est transcrit en ARN messager dans le noyau, puis expulsé dans le cytoplasme où a lieu sa traduction en protéines. 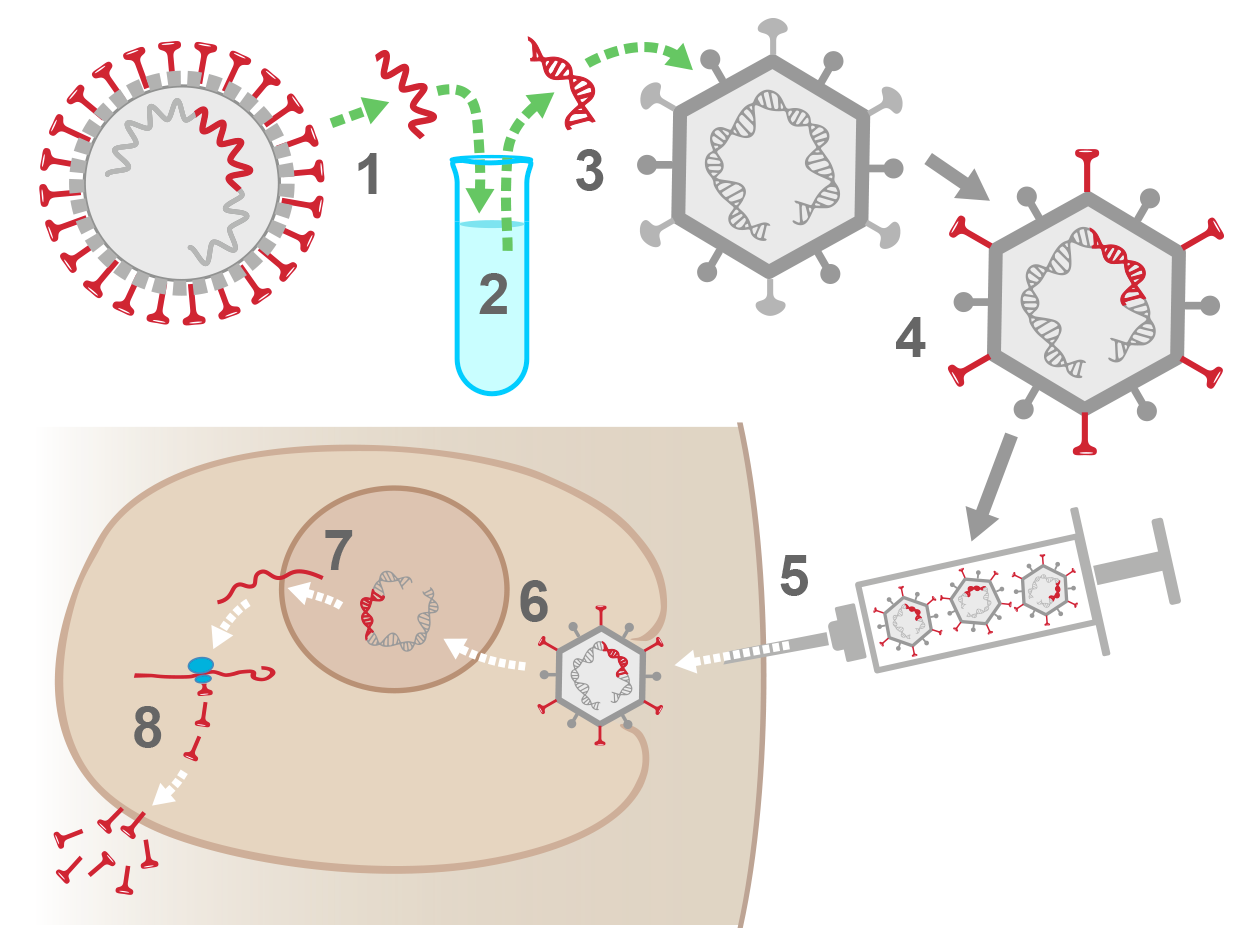 1. En laboratoire, on extrait la séquence de l'ARN du coronavirus qui contient l'information pour fabriquer sa protéine de surface Spike (en rouge).
1. En laboratoire, on extrait la séquence de l'ARN du coronavirus qui contient l'information pour fabriquer sa protéine de surface Spike (en rouge).
2. La séquence d'ARN-Spike est convertie en séquence ADN-Spike.
3. La séquence ADN-Spike est insérée dans le chromosome d'un adénovirus.
4. L'adénovirus modifié arbore la protéine de surface Spike, mais est incapable de se multiplier.
5. Vaccination: des adénovirus modifiés sont injectés dans le bras d'une personne.
6. L'adénovirus modifié pénètre dans une cellule humaine et transfère son ADN dans le noyau de celle-ci. L'ADN vaccinal est modifié pour ne pas s'intégrer dans le génome.
7. Dans le noyau, la séquence ADN-Spike est transcrite en ARN-messagers qui sortent ensuite du noyau.
8. Les outils de la cellule humaine lisent les ARN-messager, fabriquent des protéines Spike et les rejettent dans l'organisme – ce qui va alerter le système immunitaire et permettre au corps de produire des anticorps contre la protéine Spike.
2-3 semaines après la vaccination, si un coronavirus pénètre dans le corps, le système immunitaire saura le reconnaître rapidement et le neutraliser, notamment à l’aide d’anticorps contre la protéine Spike.
Vidéos de Swissmedic présentant le fonctionnement des vaccins à vecteur viral.
Par quelles étapes les candidats-vaccins doivent-ils passer avant de pouvoir être utilisés ?
Une fois un candidat-vaccin développé (voir ci-dessus), il doit passer par plusieurs phases de développement.
Les essais précliniques (sur des animaux) sont généralement réalisés sur des rongeurs, puis sur des singes. C’est une étape indispensable pour sélectionner les meilleurs candidats et éviter d’administrer à des humains des vaccins inefficaces ou trop inflammatoires. Ces essais peuvent souvent donner d'excellents résultats chez l’animal, mais pas forcément chez l’être humain.
Les essais cliniques (chez l’humain) se déroulent en quatre phases:
- Les essais de Phase I ont lieu généralement sur quelques dizaines de volontaires. Ils ont pour but d’observer les effets secondaires éventuels très fréquents (en comparaison avec un placebo ou un vaccin connu). Ils permettent aussi de déterminer la dose optimale du vaccin expérimental, en mesurant les anticorps produits par les volontaires.
- Les essais de Phase II élargissent les connaissances, en incluant plusieurs centaines ou des milliers de volontaires, dans plusieurs centres cliniques différents. Les volontaires sont suivis pendant plusieurs mois, notamment pour observer l’évolution, dans le sang, de leurs taux d’anticorps ou de lymphocytes B et T. Cette étape permet d’étudier les détails de la réponse immunitaire, de préciser les schémas d’administration (nombre de doses, etc.) et d’identifier les effets secondaires fréquents.
- Les essais de Phase III incluent plusieurs dizaines, voire des centaines de milliers de volontaires. Ils visent à déterminer si le vaccin protège contre la maladie. Il s’agit donc d’observer dans quelle mesure les personnes vaccinées exposées au microbe résistent à la maladie dans les semaines ou les mois suivant la vaccination. Ces essais à grande échelle sont les seuls capables de détecter les effets secondaires rares, ainsi que de définir dans quelles classes d’âge ou groupes de population le candidat-vaccin est efficace - ou non.
- Les essais de Phase IV sont réalisés après la commercialisation d’un vaccin pour préciser son utilisation auprès de populations qui n’avaient pas été incluses dans les essais de phase II et III. Il s’agit aussi de vérifier si des effets indésirables très rares, mais graves, surviennent chez les millions de personnes vaccinées.
Qui décide si un vaccin peut être mis sur le marché ?
Pour sa mise sur le marché, un vaccin doit obtenir l’homologation des autorités de régulation chargées de la sécurité des produits pharmaceutiques. Le fabricant doit présenter un dossier complet aux autorités de régulation (Swissmedic en Suisse, l’EMA en Europe, la FDA aux USA et l’OMS pour le monde entier). Le fabricant doit également démontrer sa capacité à produire le vaccin en toute sécurité et à grande échelle.
Pour qu’un vaccin puisse être produit en masse, les laboratoires qui développent des vaccins doivent souvent s’associer à une ou plusieurs grandes entreprises pharmaceutiques spécialisées disposant des moyens techniques nécessaires.
Avant qu’un lot de vaccin soit mis sur le marché, le fabricant doit le soumettre à l’autorité de régulation pour approbation, afin qu’elle en juge la qualité, la sécurité et son impact sur le système immunitaire. Ainsi, les autorités de régulation sont non seulement responsables d’analyser la sécurité des vaccins, mais aussi d’autoriser leur mise sur le marché.
Qui décide si un vaccin devrait être recommandé, à qui et comment ?
Cette étape est du ressort des autorités de santé chargées des recommandations vaccinales (en Suisse, la Commission fédérale pour les vaccinations et l’OFSP - Office fédéral de la santé publique).
La vaccination contre une maladie est recommandée uniquement si le bénéfice dépasse nettement le risque d'effets indésirables. La décision repose sur un cadre analytique. Contre une même maladie, il est possible d’utiliser plusieurs vaccins qui ont été approuvés par Swissmedic. La Commission fédérale pour les vaccinations peut alors recommander l’utilisation d’un vaccin plutôt qu’un autre, en fonction des caractéristiques de la population. C’est elle qui détermine à qui (âge, facteurs de risque) le vaccin est recommandé, en combien de doses et à quelles fréquences il faut l’administrer, et quand un rappel est nécessaire en fonction des risques de maladies dans le pays, etc.
Les autorités de santé (OFSP) sont aussi chargées de négocier les coûts du vaccin avec les producteurs.
Toutes les phases du développement jusqu'à la commercialisation d’un vaccin durent, en moyenne, de 10 à 20 ans – et parfois même plus. Mais lorsqu’il y a urgence, il est possible de raccourcir ces délais, comme cela a été fait dans le développement de vaccins contre la maladie d’Ebola ou le Covid-19.

